
خانه » آزمایش اندازه گیری نقطۀ جوش

آزمایش اندازه گیری نقطۀ جوش، یکی از راه های شناسایی تقریبا تمامی مایعات و برخی از جامداتی است که نقطۀ ذوب پایینی دارند و در درجۀ حرارت های کم شروع به ذوب شدن می کنند. در مقابل، جامداتی که نقطۀ ذوب بالایی دارند و در درجۀ حرارت بالا ذوب می شوند، معمولا آنقدر دیر می جوشند که نمی توان به راحتی نقطۀ جوش آنها را اندازه گیری کرد. از طرفی، بسیاری از ترکیب ها، مخصوصا آن دسته از ترکیباتی که در درجۀ حرارت بالا می جوشند، در آن دمای نقطۀ جوش استاندارد خود تجزیه می شوند. ضمن اینکه وجود ناخالصی در ترکیبات هم باعث تغییر نقطۀ جوش می شود. در این مقاله، به آزمایش اندازه گیری نقطۀ جوش می پردازیم. در صورتی که از این مقاله خوشتان آمد، خوشحال می شویم که نظرات خود را برای ما ارسال کنید.
هنگامی که به یک مایع حرارت می دهید، فشار بخار آن افزایش می یابد. این افزایش فشار بخار تا جایی ادامه می یابد که در یک درجۀ حرارت مشخص، مایع شروع به جوشیدن می کند. این نقطه، همان نقطۀ جوش آن مایع است. نقطۀ جوش هر مایع ای به طور استاندارد در فشار 760 میلی متر جیوه (یا همان یک اتمسفر) اندازه گیری می شود. در فشار های کمتر، فشار لازم برای جوشیدن نیز کمتر خواهد بود و مایع در دمای کمتری خواهد جوشید. ارتباط بین فشار بخار مایع و دمای جوش به وسیله نمودار “فشار بخار مایع بر حسب دما مایع” تعیین می شود. به شکل 1 در زیر توجه کنید:
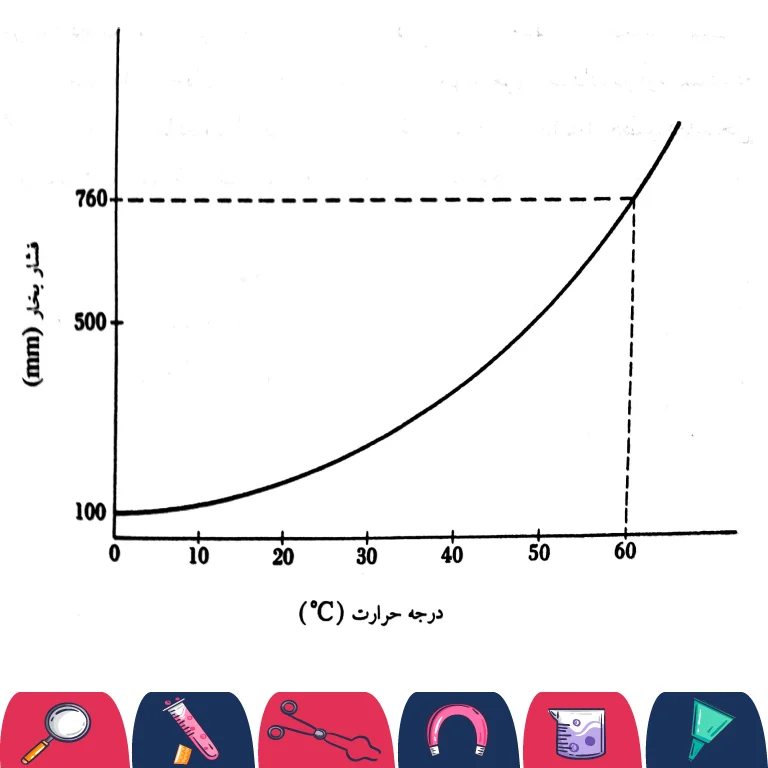
در این نمودار، برای یک مایع فرضی، یک حالت ایده آل از میزان فشار بخار مایع به ازای دماهای مختلف همان مایع نشان داده شده است. از آنجا که اندازۀ نقطۀ جوش بستگی به مقدار فشار بخار مایع دارد، در مواردی که نقطۀ جوش در ارتفاعی بالاتر یا پایین تر از سطح دریا اندازه گیری می شود، لازم است که با استفاده از یک فشارسنج، فشار نشان داده شده توسط فشارسنج را یاداشت کنید. اگر نقطۀ جوش در فشار کم اندازه گیری شود، مانند مواردی که از پمپ خلأ یا خرطوم آبی استفاده می شود، باز باید فشار قرائت شده از فشارسنج را یاداشت نمود. به عنوان یک قاعدۀ تقریبی، نقطۀ جوش بسیاری از مایعات در حوالی فشار 760 میلی لیتر جیوه، به ازای هر 10 میلی لیتر جیوه کاهش فشار، حدود نیم درجه سانتیگراد کاهش می یابد. در فشار های پایین تر، به ازای هر بار نصف شدن فشار، نقطۀ جوش 10 درجه سانتیگراد کاهش می یابد. برای نمونه اگر نقطۀ جوش مشاهده شده برای یک مایع در فشار 10 میلی لیتر جیوه برابر 150 درجۀ سانتیگراد باشد، نقطه جوش آن در 5 میلی لیتر جیوه حدود 140 درجۀ سانتیگراد خواهد بود.
اکنون مایعی را در نظر بگیرید که در درجۀ حرارت معینی، در ظرف سرگشاده ای (سر باز) قرار دارد و مولکول های فاز بخار در بالای مایع می توانند از فضای ظرف به بیرون خارج شوند. بخاری که در بالای این مایع است از مولکول های هوا و مولکول های مایع تشکیل شده است.
طبق قانون فشار های جزئی دالتون، فشار کل (خارجی) در بالای مایع برابر با فشارهای جزئی نمونه و هواست.
Ptotal = Psample + Pair
فشار جزئی نمونه برابر با فشار بخار حالت تعادلی مایع در درجۀ حرارت معین است. اگر درجۀ حرارت بالا رود، بدین ترتیب فشار بخار حالت تعادلی مایع زیاد شده، تعداد مولکول های نمونه در فضایی که در بالا و نزدیک مایع است، افزایش می یابد. در نتیجه مقداری از هوا جا به جا می شود. در درجۀ حرارت بالا در فشار جزئی نمونه، درصد بیشتری از فشار کل را تشکیل می دهد. با ازدیاد بیشتر درجۀ حرارت، این عمل ادامه می یابد تا فشار بخار حالت تعادلی با فشار خارجی برابر شود و در این حال تمام هوا کاملا از ظرف خارج می شود. تبخیر بیشتر باعث جا به جا شدن مولکول های گازی نمونه خواهد شد. فشار بخار تعادلی نمونه یک حد نهایی داردکه به وسیله فشار داخلی معین می شود. در این حد سرعت تبخیر به مقدار زیادی افزایش می یابد (با تشکیل حباب در مایع آشکار می شود). این مرحله را معمولا شروع جوشش می دانند. نقطۀ جوش یک مایع درجه حرارتی است که در آن فشار بخار مایع کاملا برابر با فشار خارجی می شود. معمولا نقطۀ جوش استاندارد را در فشار یک اتمسفر در نظر می گیرند.
دو روش ساده برای تعیین نقطۀ جوش وجود دارد. هنگامی که مقدار زیادی از نمونه در دست باشد می توان به راحتی نقطۀ جوش (یا دامنۀ جوش) را از طریق دماسنج طی یک عمل تقطیر ساده به دست آورد. برای تعیین نقطۀ جوش در مواقعی که مقدار نمونه کم است، از روش میکرو می توان استفاده کرد. در شکل 2 وسایل آزمایشگاهی مورد نیاز نشان داده شده است.

برای انجام روش میکرو، یک قطعه لوله شیشه ای 5 میلی متری را که یک طرف آن بسته شده، به وسیله یک حلقۀ لاستیکی، یا یک قطعه لولۀ لاستیکی خیلی کوتاه به دماسنج متصل می کنند.
مایعی را که نقطۀ جوش آن باید تعیین شود، توسط پیپت یا قطره چکان درون این لوله می ریزند و یک قطعۀ کوچک از لولۀ مویین (که یک طرف آن بسته است) از طرف باز آن (یعنی وارونه) درون این لولۀ بزرگتر قرار می دهند. سپس تمام این مجموعه را در یک لولۀ تیل (Thiele) یا یک بشر کوچک حاوی پارافین مایع قرار می دهند. حلقۀ لاستیکی باید بالای سطح پارافین مایع باشد. در غیر این صورت امکان شل شدن آن در پارافین مایع داغ وجود دارد. هنگام قرار دادن حلقۀ لاستیکی باید به خاطر سپرد که پارافین مایع در اثر گرم شدن منبسط می شود و سپس لولۀ تیل یا بشر را حرارت می دهند، تا وقتی که یک جریان سریع و پیوسته از حباب های گاز از درون لولۀ مویین وارونه خارج شود. در این لحظه باید گرم کردن را متوقف کرد. جریان حباب ها در ابتدا سریع بوده و پس از مدتی آرام می شود و در انتها خروج حباب ها متوقف می شود. پس از توقف حباب ها، مایع وارد لولۀ مویین می شود. لحظه ای که مایع شروع به ورود به لولۀ مویین می کند با نقطۀ جوش مایع مطابقت دارد، بنابراین باید دمای مربوط را ثبت کرد.
در خلال گرم کردن اولیه، هوای محبوس در لولۀ مویین منبسط شده و از آن خارج می شود و جریانی از حباب ها را ایجاد می کند. هنگامی که عمل گرم کردن متوقف شد، تنها بخاری که وارد لولۀ مویین می شود، از مایع گرم شده ای که با انتهای لولۀ مویین در تماس است، حاصل شده است. از آنجا که همیشه بین بخار و مایع گرم شده تعادل وجود دارد، اگر دمای مایع بالاتر از نقطۀ جوش آن باشد، فشار بخار محبوس بیشتر یا برابر فشار اتمسفر خواهد بود. در حالی که مایع سرد می شود، فشار بخار آن نیز کاهش می یابد. همین که فشار بخار مایع به پایین تر از فشار اتمسفر رسید، مایع بر اثر اختلاف فشار وارد لولۀ مویین می شود.
به طور کلی در این روش دو اشکال پیش می آید. نخست وقتی که مایع آنقدر سریع گرم شود که تمام آن تبخیر شود و دیگر هنگامی که نتوان مایع را تا بالاتر از نقطه جوش گرم کرد. اگر گرم کردن در پایین تر از نقطۀ جوش مایع متوقف شود، مایع سریع وارد لوله خواهد شد، زیرا که بخار محبوس فشارش کمتر از فشار اتمسفر است. نقطۀ جوش مشاهده شده از روی دماسنج، طبق روش تقطیر یا روش میکرو اغلب پایین تر از نقطۀ جوش واقعی است. این شکل به ویژه در اندازه گیری دما های بالاتر از 150 درجۀ سانتیگراد واقعیت پیدا می کند. سازندگان دماسنج ها بیشتر آنها را طوری طراحی می کنند که وقتی در محیط اندازه گیری دما غوطه ور هستند دمای صحیح را نشان می دهند.
روش میکرو در صورتی نتایج مطلوب دارد که به طور دقیق کار شود، فقط افراد دقیق نتایج خوبی را با این روش به دست می آورند. در صورتی که بدون دقت این عمل انجام گیرد نقطه جوش ممکن است با خطای برابر 5 درجه یا بیشتر همراه باشد.
آزمایش اندازه گیری نقطه جوش، یکی از آزمایش های بسیار رایج در حوزه های مختلف است. امروزه بسیاری از صنایع شیمیایی و دارویی نقطه جوش را با شیوه های رایج اندازه گیری کرده و به مشتریان خود این اطلاعات را ارائه می دهند. اگر از توضیحات این مقاله رضایت داشتید، ممنون می شویم نظرات خود را در انتهای این مقاله برای ما ارسال کنید. مجله شیمیکال برای توسعه کیفیت کاری خود، همواره نیازمند نقطه نظرات شما عزیزان است.

از سال 1392 که وارد دانشگاه در مقطع لیسانس شدم، همیشه در حال مطالعه فیزیک و شیمی به صورت خودخوان بودم و هستم. این علاقه بی کران من به علم تا به امروز ادامه دارد و هیچ وقت از آموختن مطالب جدید خسته نمی شوم. شیمیکال مارکت برای من جایی است که بتوانم هم از علم کسب درآمد کنم و هم دانسته های خود را با شما به اشتراک بزارم. دانش، اعتبار است.
تهران ، ملارد ، بلوار مارلیک ، خیابان پرنیان ، کوچه مریم غربی ، پلاک 91 ، واحد 8
تهران ، ملارد ، بلوار مارلیک ، جنب بانک مسکن ، پاساژ امیر
3176196665
02165165346
09202033170
09202033170
sales@shimikal.com
09128909623
a.alinejad@shimikal.com
09304900214
support@shimikal.com
hr@shimikal.com
شنبه تا چهارشنبه 9 الی 17 - پنجشنبه ها 9 الی 13
مطالعه نکات عنوان شده در ذیل قبل از ثبت اطلاعات و یا تماس با ما ضروری است.
ویژه خریداران
1- قبل از ثبت اطلاعات حتما از صحت اطلاعات وارد شده اطمینان حاصل نمایید.
2- اطلاعات شما پس از ثبت توسط سیستم پردازش شده و حداکثر ظرف 10 دقیقه در جدول مشتریان نمایش داده می شود.
3- از ارسال درخواست های مکرر و پشت سر هم اکیدا خوداری کنید. زیرا سیستم امنیتی سایت ip شما را مسدود کرده و دسترسی شما به سایت متوقف خواهد شد.
4- اگر ظرف یک روز کاری از طرف همکاران و سایر فروشندگان درخواست شما پاسخی نگرفت، مراتب را به آدرس info@shimikal.com اطلاع داده تا در اسرع وقت درخواست شما به فروشنده دیگری ابلاغ شود.
ویژه فروشندگان و همکاران
1- تنها مرجع ارتباطی شما info@shimikal.com است. در صورت نیاز می توانید در مواقع ضروری با شماره تلفن وب سایت 02165165346 تماس بگیرید.
2- به دلیل قوانین حریم خصوصی کاربران وب سایت، شیمیکال مارکت از دادن اطلاعات هویتی و شخصی کاربران اکیدا منع شده است. لطفا از ما اطلاعات کاربران را درخواست نفرمایید.
3- سامانه خرید و فروش شیمیکال مارکت نوعی پل ارتباطی بین فروشندگان و خریداران است و در قبال ایجاد این پل ارتباطی هیچگونه کمیسیون و سودی از طرفین معامله دریافت نمی شود.
4- اگر معامله ای توسط سامانه خرید و فروش شیمیکال مارکت با موفقیت به اتمام برسد، شیمیکال مارکت متعهد می شود که اطلاعات تمامی طرفین معامله (خریدار و فروشنده) را به کلی حذف کرده و در حفظ مشتریان برای همکاران و فروشندگان هم صنفی کوشا باشد.
5- برای تمام فروشندگان و همکاران عقد قرارداد همکاری به صورت رسمی و حضوری الزامی است. در خصوص نحوه عقد قرارداد با ما تماس بگیرید.
قبل از ارسال درخواست استعلام قیمت به مطالب زیر توجه کنید:
1- از صحت اطلاعات وارد شده اطمینان حاصل نمایید.
2- لطفا از ارسال اطلاعات دیگر افراد خوداری نمایید.
3- همکاران ما بعد از حداقل 24 ساعت و حداکثر 72 ساعت با شما تماس خواهند گرفت.
4- بعد از ارسال اطلاعات به ایمیل شما یک پیش فاکتور رسمی در قالب pdf ارسال خواهد شد. پس الزامی است که از صحت ایمیل وارد شده اطمینان حاصل نمایید.
5- لطفا از ارسال درخواست های مکرر پرهیز کنید.
6- بعد از ارسال هر درخواست حداقل 24 ساعت برای پردازش درخواست شما زمان است.
7- به دلیل نوسانات قیمت ارز در کشور، تاریخ انقضای هر پیش فاکتور فقط 24 ساعت می باشد.
8- قبل از ارسال درخواست استعلام قیمت، محصول مورد نظر خود را در صفحه فروشگاه جستجو کنید.