
خانه » نقطه ذوب: روش اندازه گیری و اثر ناخالصی ها در نقاط ذوب مخلوط ها

نقطه ذوب (به انگلیسی: Melting Point) یکی از ثابتهای فیزیکی است که در تشخیص ماهیت مواد آلی مورد استفاده قرار میگیرد. زیرا هر ترکیب آلی به صورت جامد نقطه ذوب مشخصی دارد و کمتر دو ترکیب آلی ای یافت میشوند که نقطه ذوب یکسان داشته باشند. یکی از روش های تعیین خلوص ترکیبات بلوری در آزمایشگاه شیمی آلی، اندازه گیری نقطه ذوب است. نقطه ذوب در آزمایشگاه توسط یک وسیله مخصوصی که مجهز به دماسنج، سیستم مقاومت الکتریکی و حمام حرارتی است، اندازه گیری می شود. در آن وسیله، مقدار کمی از ماده بلوری مورد نظر را به آرامی حرارت میدهند و با استفاده از دماسنج، تغییرات دما را در دو نقطه میخوانند.
فاصله بین این دو نقطه را دامنه ذوب می نامند. مثلاً اگر نقطه ذوب یک ماده از 51 تا 54 درجه سانتی گراد باشد، آن ماده در فاصله 3 درجه سانتی گراد ذوب میشود.
نقطه ذوب یک ماده خالص، درجه حرارتی است که آن ماده همزمان در فازهای مایع و جامد (بدون تغییر درجه حرارت) وجود داشته و در حال تعادل باشد. اگر ماده خالصی در نقطه ذوب باشد، چنانچه به مخلوط فازهای جامد و مایع آن ماده حرارت داده شود، تمام فاز جامد به فاز مایع تبدیل شده و اصطلاحاً ماده ذوب می شود. برعکس این فرآیند بدین گونه است که اگر میزان حرارت از مخلوط فازهای جامد و مایع کاهش یابد، تمام فاز مایع به فاز جامد تبدیل شده و اصطلاحاً ماده منجمد می شود.
پس با این تفاسیر برای یک ماده خالص، ما می توانیم آن درجه حرارتی را که ماده ذوب می شود (نقطه ذوب) را همان درجه حرارتی که ماده خالص منجمد می شود (نقطه انجماد) عملاً یک نقطه در نظر بگیریم.
به نمودار زمان بر حسب درجه حرارت که شکل زیر نشان داده شده، توجه کنید.
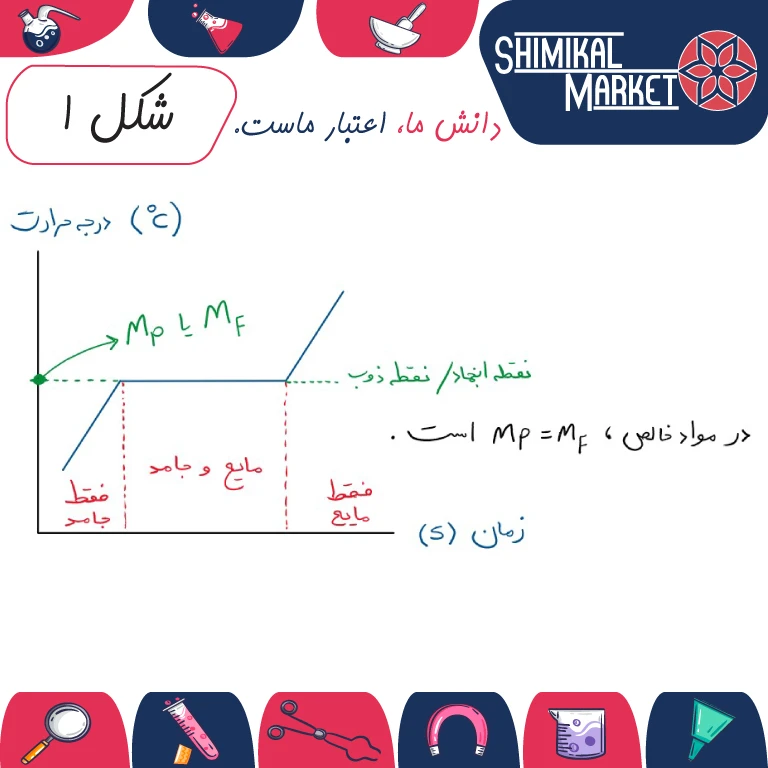
در این نمودار رابطه بین فازهای جامد و مایع برای یک ترکیب خالص را می توانید مشاهده کنید. توجه داشته باشید که حرارت باید با سرعت ثابتی افزایش و یا کاهش یابد. در غیر این صورت نمودار ما از حالت خطی خود خارج می شود. در درجه حرارت های پایین، ماده خالص به صورت فاز جامد است و افزایش گرما موجب بالا رفتن درجه حرارت آن میشود.
هنگامی که نقطه ذوب فرا میرسد اولین مقدار جزئی از فاز مایع بر روی سطح ظاهری ماده خالص با فاز جامد نمایان میشود. برای درک بهتر، از شرکت Loba Chemie محصول استون با در صد خلوص 99.9 درصد با گرید GC یا همان کروماتوگرافی گازی را انتخاب می کنیم. مشخصات این محصول به شرح زیر است:
| کد محصول | گرید | درصد خلوص |
| 0013A | کروماتوگرافی گازی | 99.9 |
| CAS No | نقطه ذوب / نقطه انجماد | حالت فیزیکی در 20 درجه سانتی گراد |
| 67-64-1 | 95.35- درجه سانتی گراد | مایع |
نقطه ذوب (دامنه ذوب) به دو صورت درجه خلوص یک ماده را مشخص میکند. اول اینکه هر قدر ماده خالصتر، نقطه ذوب آن بالاتر و دامنه نقطه ذوب آن کوتاهتر است. افزودن مقدار قابل توجهی از یک ناخالصی به یک ماده خالص، معمولاً سبب کاهش نقطه ذوب (بر حسب میزان ناخالصی) میشود. زیرا نقطه انجماد یک ماده وقتی که یک ماده خارجی به آن اضافه شود پایین میآید. نقطه انجماد همان نقطه ذوب است، با این تفاوت که این عمل در جهت عکس انجام میشود. در شکل زیر رفتار معمولی نقطه ذوب در مورد مخلوطهای متفاوتی از دو ماده الف و ب مشاهده میشود.
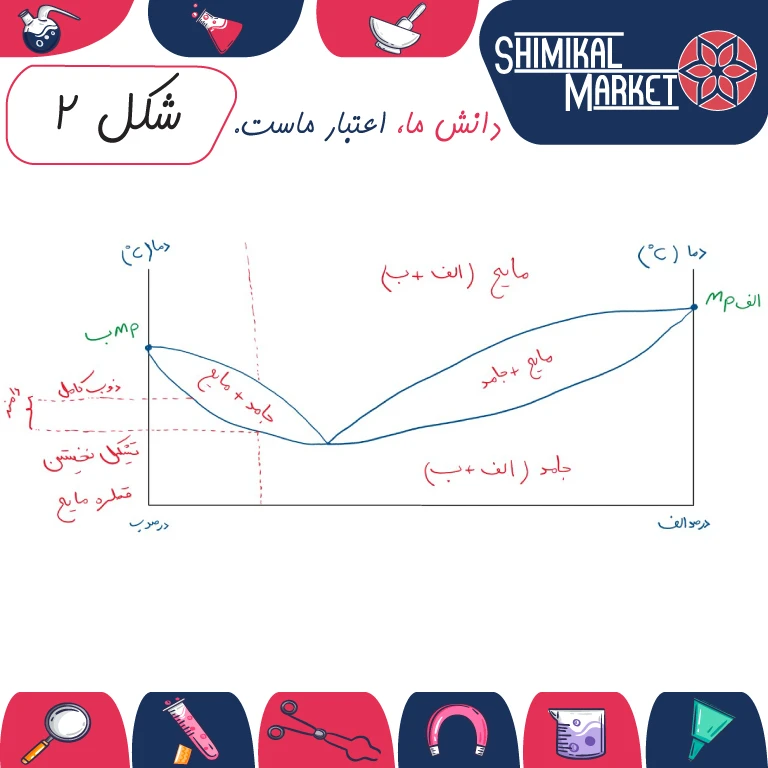
گزاره 1 و 2 صرفا به ما می گوید که اگر یک نقطه از محور افقی را انتخاب کردید، خط عمود بر آن نقطه محور ما را در حداقل یک و حداکثر دو نقطه قطع می کند. به تصویر زیر نگاه کنید. یک نقطه فرضی K را در محور افقی نمودار (که بیانگر میزان درصد وزنی هر کدام از مواد الف و ب است) انتخاب نموده ایم.
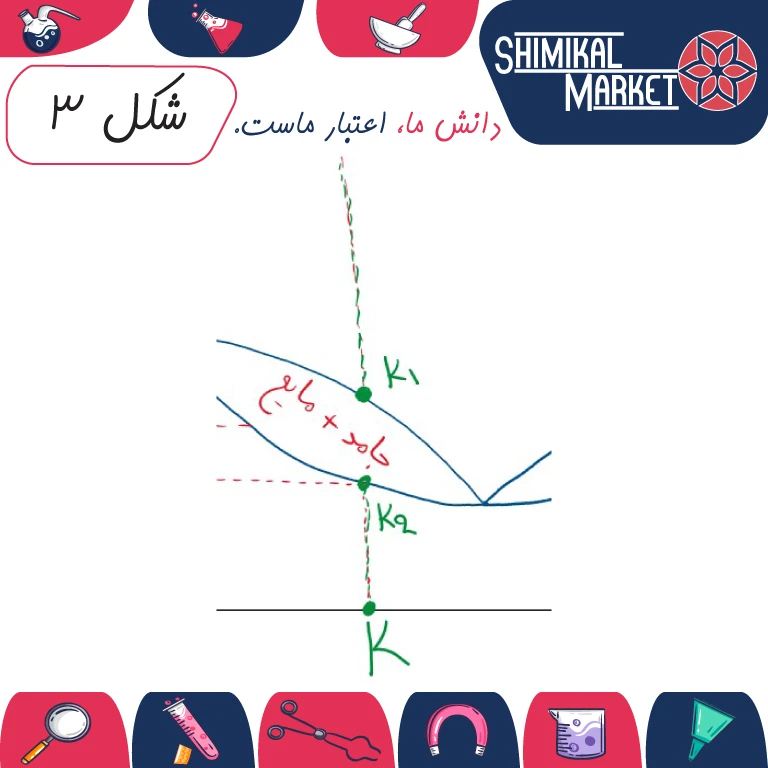
نقطه k نمودار را در دو نقطه k1 و k2 قطع می کند. نقطه k1 همان دمایی است که نمونه ما (که حاوی درصد مشخصی از ماده الف و ب است) شروع به ذوب شدن می نماید. تصویر نقطه k1 بر روی محور عمودی سمت راست دمایی است که ماده الف در آن شروع به ذوب شدن می نماید و تصویر نقطه k1 بر روی محور عمودی سمت چپ دمایی است که ماده ب شروع به ذوب شدن می نماید. همینطور نقطه k2 نیز دمایی است که نمونه ما به طور کامل ذوب شده است و در فاز مایع قرار دارد و تصویرش بر دو محور عمودی، همان معانی گفته شده برای نقطه k1 را می دهد.
اگر از ماده خالص الف شروع کنیم و با افزایش ناخالصی ب، نقطه ذوب کاهش مییابد. دامنه ذوب را در این نمودار، حد فاصل بین k1 و k2 تعیین می کند. این مثال این نکته را روشن میسازد که در مخلوطهایی که شامل مقادیر کم از ناخالصی (یعنی کمتر از 15%) هستند، دامنه نقطه ذوب اغلب نشانه میزان خلوص است. مادهای که ذوب آن در دامنه کوچکی انجام میشود، به طور عادی باید خالص باشد. شاید برایتان سوال باشد که در نقطه ای که در شکل زیر با E نشان می دهیم، چه اتفاقی در حال رخ دادن است؟
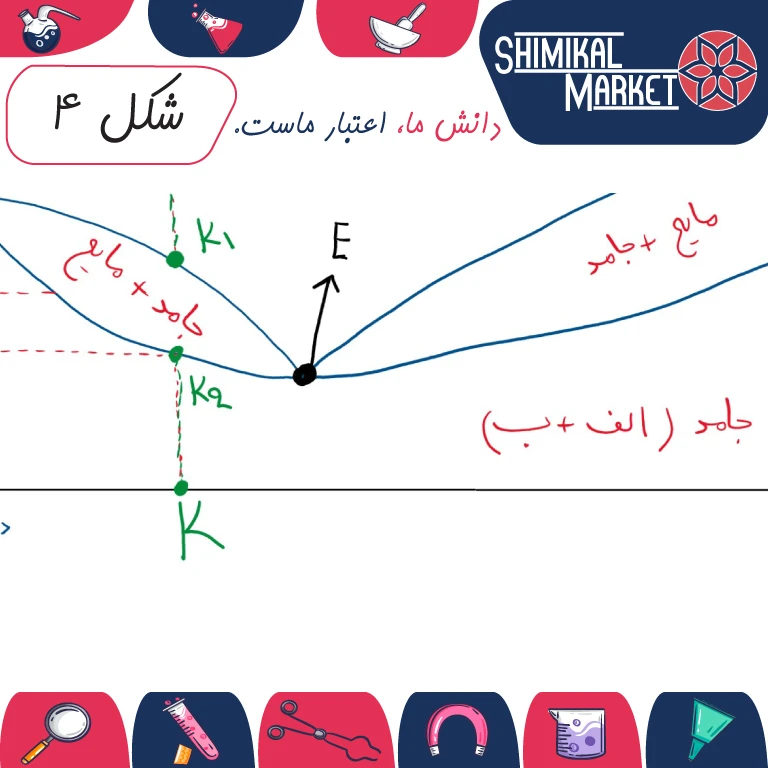
نقطهای که در آن چهار نمودار یکدیگر را قطع میکنند، نقطهی یوتکتیک (Eutectic Point) نام دارد. این نقطه به دمایی خاص و ترکیب مشخصی از دو ماده (الف و ب) اشاره دارد که در آن، جامد مستقیماً به مایع تبدیل میشود و بالعکس، بدون اینکه یک فاز میانی (جامد+مایع) وجود داشته باشد.
در این نقطه، تمام نمونه شامل مخلوط الف و ب در حالت جامد، بهطور همزمان و کامل به حالت مایع تبدیل میشوند. این یعنی، نمونه نه کاملاً جامد است و نه در حالتی است که فقط بخشی از آن ذوب شده باشد.
دما در این نقطه ثابت است، حتی اگر حرارت اضافه شود یا از آن گرفته شود، تا زمانی که کل نمونه تغییر فاز دهد (ذوب یا انجماد).
این نقطه تنها برای ترکیب خاصی از دو ماده (مثلاً درصد مشخصی از الف و ب) وجود دارد. در ترکیبهای دیگر، چنین رفتاری مشاهده نمیشود.
در دمای یوتکتیک و ترکیب مشخص، سیستم در حالتی است که جامد و مایع بهطور همزمان وجود دارند و تغییر فاز سریع انجام میشود.
بنابراین، بسته به شرایط:
این نقطه اهمیت زیادی در متالورژی، شیمی و مهندسی مواد دارد، زیرا فرآیندهای تغییر فاز در آن سادهتر و سریعتر رخ میدهند. از آنجا که همه مخلوطهای دوتایی تشکیل نقطه یوتکتیک نمیدهند، در مورد این فرض که “هر مخلوط دوتایی رفتاری مشابه آنچه در بالا گفته شد دارد”، باید کمی محتاطانه صحبت کرد. حتی جالب است بدانید که بعضی ترکیبات بیش از یک نقطه یوتکتیک تشکیل میدهند. علی رغم این حالتهای مختلف نقطه ذوب و دامنه آن هر دو شاخص مفیدی برای خلوصاند و تقریباً به راحتی تعیین میشوند.
شکل زیر نمودار فاز مربوط به رفتار یک مخلوط دو جزئی معمولی (الف + ب) را در ذوب شدن نشان میدهد.
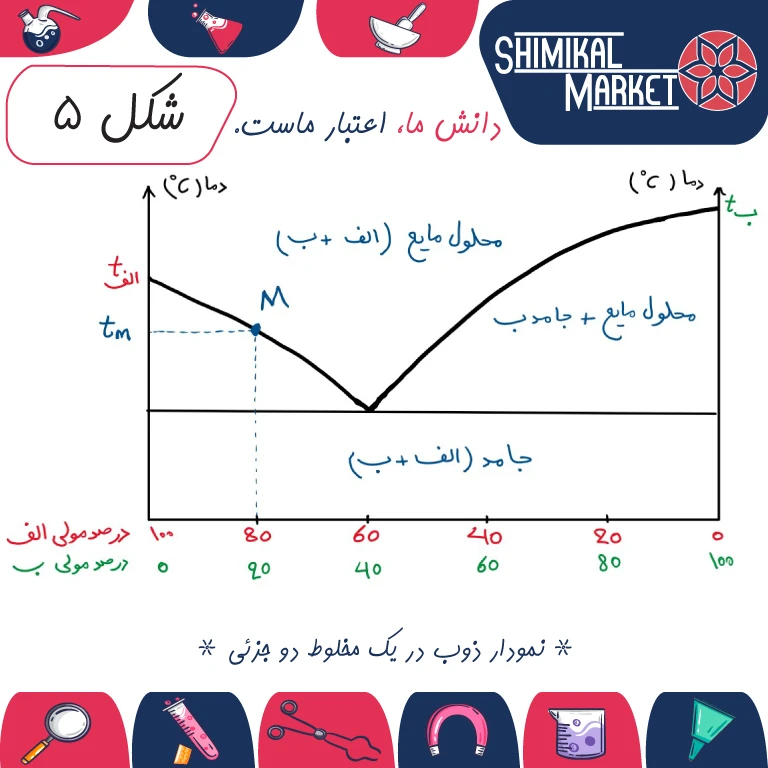
تغییرات نقطه ذوب بستگی به مقدار ماده نسبی الف و ب در مخلوط دارد. اگر ماده الف یک ماده خالص باشد (بدون ب)، در نقطه ذوب خود tA به طور ناگهانی ذوب میشود. در صورتی که ماده ب یک ماده خالص باشد، آن هم در tB ذوب میشود که در سمت راست نمودار مشخص شده است. در نقاط tA و tB جامد خالص در یک دامنه کوچک از دما، از جامد به مایع تبدیل میشود. اما در مخلوط دو ماده الف و ب موضوع فرق میکند. با استفاده از شکل فوق مخلوطی شامل ۸۰ درصد از ماده الف و ۲۰ درصد از ماده ب را بر حسب درصد مولی در نظر بگیرید. نقطه ذوب این مخلوط در دمای tM به وسیله نقطه M روی نمودار نشان داده شده است. یعنی با افزایش درصد مولی ماده ب، نقطه ذوب ماده الف از tA به tM نزول می کند.
از پایین آمدن نقطه ذوب که در اثر ورود ناخالصی در ترکیب خالص به وجود میآید، میتوان در شناسایی نوع ترکیب استفاده کرد. نام این روش مهم « اندازهگیری نقاط ذوب مخلوط یا Mixed Melting Point » (به اختصار MMP) نام دارد. شاید این موضوع در قالب یک مثال بتواند برای شما خواننده عزیز بهتر و شفاف تر بیان شود:
فرض کنید که ترکیبی در 133 درجه سانتی گراد ذوب میشود و شما حدس می زنید که این ترکیب یا اوره و یا سینامیک اسید ترانس می تواند باشد. زیرا که هر دو در 133 درجه سانتی گراد ذوب میشوند. چنانچه این ترکیب با اوره خاص کاملاً مخلوط شود و معلوم شود که نقطه ذوب مخلوط حاصل از نقطه ذوب اوره خالص کمتر است، در این صورت می توان فهمید که اوره مانند یک ناخالصی عمل کرده و ترکیب مورد نظر ما نمیتواند اوره باشد.
از طرفی دیگر، در صورتی که نقطه ذوب مخلوط با نقطه ذوب ترکیب مورد نظر ما یکسان شود، می توان پیش بینی کرد که به احتمال قوی ترکیب مورد نظر ما اوره است.
آزمایش تعیین نقطه ذوب در شیمی آلی به مقدار کافی ماده نیاز دارد تا با گرم و سرد کردن متناوب، تعادل بین فازهای مایع و جامد برقرار شود. اما اغلب این مقدار در آزمایشگاه موجود نیست. از این رو روشهای میکرو (که چندان هم دقیق نیستند) و با مقدار ناچیزی از ماده قابل انجام هستند، توسعه یافتند. از معمولترین روشهای میکرو میتوان به روش اندازه گیری نقطه ذوب با استفاده از لوله مویین اشاره کرد. در تمامی روشهای میکرو عملاً نقطه ذوب را به صورت حدود تغییرات دمای ذوب اندازه میگیرند. چنانچه این عمل با یک ترکیب بلوری خالص به صورت صحیح انجام شود، حدود تغییرات دمایی که مشاهده میشود نباید بیشتر از نیم تا یک درجه باشد. اما باید به این نکته اشاره کرد که تعداد کمی از ترکیبهای شیمیایی موجود در بازار چنین تغییرات ذوب محدودی را از خود نشان میدهند.
در اندازهگیری نقطه ذوب با لوله مویین از وسایل آزمایشگاهی گوناگون میتوان استفاده کرد. اقتصادی ترین وسایل مورد نیاز می تواند شامل یک بشر ساده که در آن مایعی با نقطه جوش بالا و در حال گرم شدن با چراغ گازی است، باشد. از طرفی، پیشرفته ترین وسایل مورد نیاز میتواند شامل گرم کننده های الکتریکی و همزن های مکانیکی باشد. از جمله موادی که معمولاً برای تهیه محلولهایی که گرمای لازم را به طور یکنواخت به لوله مویین منتقل کنند، می توان به گلیسیرین، پارافین، اتیلن گلایکول و سولفوریک اسید غلیظ اشاره کرد. مرسوم ترین آن ها در آزمایشگاه معمولا حمام پارافین است. در صورتی که ازسولفوریک اسید استفاده شد، اگر سولفوریک اسید بعد از مدتی تیره رنگ شد کمی به آن پتاسیم نیترات اضافه میشود تا بیرنگ شود.
در موقع کار با سولفوریک اسید حتماً باید از عینک ایمنی استفاده کرد و نکات ایمنی آزمایشگاه را رعایت نمود. برای آنکه حرارت یکسان به دماسنج و لوله مویین (حاوی ماده مورد آزمایش) برسد از دستگاهی به نام لوله تیل که در شکل زیر نشان داده شده است، استفاده میشود. (جهت خرید لوله تیل کلیک کنید.)

این وسیله یک لوله شیشهای است که برای قرار دادن روغن و دماسنجی در تماس با با لوله مویین حاوی نمونه طراحی شده است. هندسه لوله تیل طوری است که اجازه جابجایی روغن گرم شده در آن را میدهد و در نتیجه باعث توزیع یکنواخت دما در تمام روغن موجود در لوله میشود. شاخه جانبی لوله برای تولید این جریانهای جابجایی طراحی شده است تا گرمای شعله را به سرعت به درون روغن گرم شده منتقل کند. شعله چراغ باید به حدی باشد که درجه حرارت دماسنج در هر دقیقه ۱ تا ۲ درجه سانتیگراد بالا برود.
ابتدا نقطه ذوب یکی از ترکیبات (مثلاً بنزوییک اسید با نقطه ذوب 121 درجه سانتی گراد و استانیلید با 113 درجه سانتی گراد) را انتخاب میکنیم تا صرفا فقط تجربه لازم برای تعیین نقطه ذوب به دست آید. چرا که نقطه ذوب این دو ماده را ار قبل می دانیم. در مرحله اول باید از خشک بودن نمونه مورد آزمایش مطمئن شد. سپس مقدار کمی از آن را روی یک شیشه ساعت تمیز ریخته (نباید از کاغذ صافی استفاده کرد. زیرا الیاف سلولز با ترکیب مخلوط شده و به عنوان ناخالصی عمل میکند و شما هم دیگر می دانید با اضافه شدن ناخالصی چه بر سر نقطه ذوب می آید.)
نمونه را در انتهای یک لوله مویین که یک انتهای آن بسته است قرار داده و آن را حرارت میدهند. برای پر کردن لوله معین انتهای باز لوله را به آرامی در نمونه پود شده از ماده بلوری فشار میدهند. در اثر این عمل مقداری از بلور در انتهای لوله فرو خواهد رفت. مقدار جامد فرو رفته در لوله نباید بیشتر از ۱ تا ۲ میلیمتر ارتفاع داشته باشد. با زدن انتهای بسته لوله بر روی میز آزمایشگاه میتوان ماده جامد را به طرف انتهای بسته لوله هدایت کرد. ماده باید در لوله متراکم باشد.
لوله مویین را به وسیله یک کش یا بست لاستیکی کوچک به دماسنج متصل می کنیم. نمونه باید در مجاورت حباب دماسنج باشد. بست لاستیکی باید به طوری باشد که در 200 درجه سانتی گراد نیز در بالای سطح مایع گرم شده دوام بیاورد و تغییر حالت ندهد. پس از انجام این کار دماسنج به کمک چوب پنبه سوراخداری که یک طرف آن بریده شده در داخل گرمکن یا لوله تیل قرار می گیرد.
زیرا از سوراخش بتوان دماسنج را در جای خودش ثابت و فیکس کرد و منظور از بریدگی آن است که درجههای دماسنج در آن حدود آشکار شود. همچنین چیدمان سیستم آزمایش باید یک سیستم باز باشد. زیرا هرگز نباید یک سیستم بسته را حرارت داد. با استفاده از یک چراغ کوچک بنزن (چراغ گاز کوچک) درجه حرارتی را که در ابتدای عمل ذوب مشاهده میشود و همچنین درجه حرارتی را که در آن آخرین قسمت جامد ذوب میشود ملاحظه کنید و این درجهها را به عنوان حدود تغییرات ذوب یادداشت کنید. حال سوال پیش می آید که نقطه ذوب به چی بستگی دارد؟ در جواب باید گفت نقطه ذوب مشاهده شده به چندین عامل بستگی دارد:
سه عامل اول باعث میشود که نقطه ذوب مشاهده شده با نقطه ذوب حقیقی متفاوت باشد. زیرا این عوامل زمان انتقال حرارت از مایع گرم به نمونه و هدایت آن در داخل نمونه را تغییر میدهند. همچنین اگر مایع خیلی سریع گرم شود درجه دماسنج از درجه حرارت مایع عقب میماند. عواملی که باعث خطا در تعیین نقطه ذوب میشوند عبارتند از:
یکی از منابع خطا در حرارتهای بالا عبارت است از خطای حاصل از تصعید که عملاً ممکن است خطای بسیار زیادی را سبب شود. برای اطمینان از نتیجه کار بهتر است آزمایش را چند بار تکرار کرد و در صورت صحیح کار کردن نتایج حاصل، داده های به دست آمده بیش از نیم درجه با یکدیگر اختلاف نخواهند داشت. در مقالات بعدی، به دنبال دستور کاری که توصیف شد، نقاط ذوب یا حدود تغییرات اجسام و مخلوطهای زیر را اندازه گیری خواهد شد.
| نام مخلوط | نسبت یا مقدار اوره | نسبت یا مقدار سینامیک اسید |
| الف | 4 | 1 |
| ب | 2 | 1 |
| ج | 1 | 1 |
| د | 1 | 2 |
| هـ | 1 | 4 |
تنها از راه تجربه میتوان چگونگی تشخیص ذوب را آموخت و آن را از تجزیه، تغییر رنگ، نرمی نسبی و جمع شدن نمونه تشخیص داد. برخی ترکیبات هنگام ذوب شدن تجزیه میشوند و این امر اغلب با تغییر رنگ همراه است. اغلب اوقات نقطه تجزیه خود یک خاصیت فیزیکی موثق میباشد که به جای نقطه ذوب استفاده میشود. این گونه نقاط تجزیه در جداول ثابتهای فیزیکی درج شدهاند. به عنوان مثال نقطه تجزیه تیامین هیدروکلرید در جدول نقطه ذوب به صورت 248 درجه سانتی گراد آمده است که نشان میدهد این ماده در 248 درجه سانتی گراد همراه با تجزیه ذوب میشود.
بعضی مواد ممکن است در دمایی زیر نقطه ذوبشان تجزیه شوند. همچنین مواد ناپایدار در برابر گرما ممکن است در هنگام حرارت دیدن واکنش حذفی انجام داده یا به حالت بیآب تبدیل شوند. محصولات تجزیهای که بدین شکل تشکیل میشوند به شکل ناخالصی در نمونه ظاهر شده و بدین طریق نقطه ذوب ماده را به طور مصنوعی پایینتر خواهند آورد.
طبیعی است که ترکیبات بلافاصله قبل از نقطه ذوبشان نرم یا جمع میشوند. چنین رفتاری نشانه تجزیه شدن نبوده بلکه علامت تغییر ساختار بلورین نمونه است.
در مورد بعضی ترکیبات به نظر میرسد که پیش از ذوبشان عرق میکنند. این تغییرات نشانه شروع ذوب نیست ذوب واقعی هنگامی شروع میشود که اولین قطره ماده مشاهده شود و دامنه ذوب تا هنگامی که همه جامد به مایع تبدیل شود، ادامه مییابد.
شخص با تجربه به زودی فرا خواهد گرفت که چگونه نرم شدن یا خمیری شدن را از ذوب واقعی تمیز دهد.

از سال 1392 که وارد دانشگاه در مقطع لیسانس شدم، همیشه در حال مطالعه فیزیک و شیمی به صورت خودخوان بودم و هستم. این علاقه بی کران من به علم تا به امروز ادامه دارد و هیچ وقت از آموختن مطالب جدید خسته نمی شوم. شیمیکال مارکت برای من جایی است که بتوانم هم از علم کسب درآمد کنم و هم دانسته های خود را با شما به اشتراک بزارم. دانش، اعتبار است.
تهران ، ملارد ، بلوار مارلیک ، خیابان پرنیان ، کوچه مریم غربی ، پلاک 91 ، واحد 8
تهران ، ملارد ، بلوار مارلیک ، جنب بانک مسکن ، پاساژ امیر
3176196665
02165165346
09202033170
09202033170
sales@shimikal.com
09128909623
a.alinejad@shimikal.com
09304900214
support@shimikal.com
hr@shimikal.com
شنبه تا چهارشنبه 9 الی 17 - پنجشنبه ها 9 الی 13
مطالعه نکات عنوان شده در ذیل قبل از ثبت اطلاعات و یا تماس با ما ضروری است.
ویژه خریداران
1- قبل از ثبت اطلاعات حتما از صحت اطلاعات وارد شده اطمینان حاصل نمایید.
2- اطلاعات شما پس از ثبت توسط سیستم پردازش شده و حداکثر ظرف 10 دقیقه در جدول مشتریان نمایش داده می شود.
3- از ارسال درخواست های مکرر و پشت سر هم اکیدا خوداری کنید. زیرا سیستم امنیتی سایت ip شما را مسدود کرده و دسترسی شما به سایت متوقف خواهد شد.
4- اگر ظرف یک روز کاری از طرف همکاران و سایر فروشندگان درخواست شما پاسخی نگرفت، مراتب را به آدرس info@shimikal.com اطلاع داده تا در اسرع وقت درخواست شما به فروشنده دیگری ابلاغ شود.
ویژه فروشندگان و همکاران
1- تنها مرجع ارتباطی شما info@shimikal.com است. در صورت نیاز می توانید در مواقع ضروری با شماره تلفن وب سایت 02165165346 تماس بگیرید.
2- به دلیل قوانین حریم خصوصی کاربران وب سایت، شیمیکال مارکت از دادن اطلاعات هویتی و شخصی کاربران اکیدا منع شده است. لطفا از ما اطلاعات کاربران را درخواست نفرمایید.
3- سامانه خرید و فروش شیمیکال مارکت نوعی پل ارتباطی بین فروشندگان و خریداران است و در قبال ایجاد این پل ارتباطی هیچگونه کمیسیون و سودی از طرفین معامله دریافت نمی شود.
4- اگر معامله ای توسط سامانه خرید و فروش شیمیکال مارکت با موفقیت به اتمام برسد، شیمیکال مارکت متعهد می شود که اطلاعات تمامی طرفین معامله (خریدار و فروشنده) را به کلی حذف کرده و در حفظ مشتریان برای همکاران و فروشندگان هم صنفی کوشا باشد.
5- برای تمام فروشندگان و همکاران عقد قرارداد همکاری به صورت رسمی و حضوری الزامی است. در خصوص نحوه عقد قرارداد با ما تماس بگیرید.
قبل از ارسال درخواست استعلام قیمت به مطالب زیر توجه کنید:
1- از صحت اطلاعات وارد شده اطمینان حاصل نمایید.
2- لطفا از ارسال اطلاعات دیگر افراد خوداری نمایید.
3- همکاران ما بعد از حداقل 24 ساعت و حداکثر 72 ساعت با شما تماس خواهند گرفت.
4- بعد از ارسال اطلاعات به ایمیل شما یک پیش فاکتور رسمی در قالب pdf ارسال خواهد شد. پس الزامی است که از صحت ایمیل وارد شده اطمینان حاصل نمایید.
5- لطفا از ارسال درخواست های مکرر پرهیز کنید.
6- بعد از ارسال هر درخواست حداقل 24 ساعت برای پردازش درخواست شما زمان است.
7- به دلیل نوسانات قیمت ارز در کشور، تاریخ انقضای هر پیش فاکتور فقط 24 ساعت می باشد.
8- قبل از ارسال درخواست استعلام قیمت، محصول مورد نظر خود را در صفحه فروشگاه جستجو کنید.